Vi ricordate la Dott.ssa Roberta Ranieri, che per Alimentazione in Equilibrio aveva scritto un bellissimo articolo sui difetti della coagulazione in relazione alla fertilità femminile?
Oggi ci parla di diabete gestazionale, una condizione che purtroppo interessa moltissime donne in dolce attesa, e che va attentamente controllata per evitare disagi sia alla mamma che al piccolo.
Buona lettura!
*** *** ***
Il diabete gestazionale
Il diabete mellito gestazionale (Gestational Diabetes Mellitus, GDM) colpisce il 7% delle donne gravide nel mondo, con una incidenza che supera il 12% nella popolazione Indiana dove si registra una alta prevalenza. Per diabete gestazionale si intende una intolleranza al glucosio che si manifesta per la prima volta durante la gravidanza ed è generalmente ristabilita dopo il parto. Tuttavia, donne con un passato di diabete gestazionale hanno un rischio aumentato di sviluppare un diabete di tipo 2 nel corso della vita: per questo motivo sarebbe utile che mantengano una dieta adeguata anche dopo il parto.
Il diabete gestazione rappresenta un rischio per la salute della madre e del feto sia nel corso della gravidanza stessa che al momento del parto.
Gli eventi avversi legati alla madre comprendono ipertensione, preeclampsia, infezioni urinarie e aumentato rischio successivo di insorgenza diabete mellito (come precedentemente detto). Per il bambino invece è associato a macrosomia (peso del feto alla nascita superiore ai 4 kg… evento che sarebbe un problema anche in vista di un parto naturale, con aumentato rischio di lacerazioni e maggior rischio di dover procedere con cesareo), anormalità congenite e rischio di sviluppo di sindrome metabolica e obesità nel corso della vita. Non stupisce quindi l’importanza della diagnosi soprattutto in fasi precoci della gravidanza, che possa così permettere un intervento tempestivo e prevenire la comparsa di complicazioni.
Chi dovrebbe essere sottoposto a screening
L’associazione americana dei diabetologi (ADA) esclude dallo screening le donne giovani con età inferiore ai 25 anni e BMI inferiore a 25, senza storia familiare di diabete o storia clinica di intolleranza glucidica.
A tutte le altre pazienti viene quindi suggerito di fare una curva da carico di glucosio per accertarsi che non vi sia diabete: in particolare devono fare attenzione donne dopo i 38 anni, quelle in sovrappeso, quelle con PCOS o con storia familiare di diabete.
Quando fare lo screening e i fattori di rischio
Lo screening viene di norma eseguito tra la 24° e la 28° settimana di gravidanza: si pone questo periodo come limite in quanto nel secondo trimestre aumenta l’insulino-resistenza, e di conseguenza donne che non hanno l’abilità di produrre abbastanza insulina da superare questa resistenza, vedono un inevitabile aumento dei valori di insulina.
Gli ormoni placentari mediano l’insulino resistenza, che a sua volta aumenta il rischio di sviluppare il diabete nel corso della gravidanza, ciò spiega anche perché un test troppo precoce potrebbe rivelarsi poco utile. Si potrebbe fare il test anche dopo la 28^ settimana, ma una diagnosi tardiva potrebbe per alcune pazienti limitare il tempo a disposizione per intervenire sul piano metabolico.
I fattori di rischio documentati per l’insorgenza del GDM sono:
1) Obesità (BMI superiore a 30)
2) Precedenti gravidanze con diabete
3) Parenti di primo grado affetti da diabete
4) Condizioni cliniche associate a insulino-resistenza (come sindrome dell’ovaio policistico, storia di ipercolesterolemia o ipertensione).
Criteri per lo screening e per la diagnosi
Non c’è un consenso internazionale riguardo il metodo e i criteri per lo screening e la diagnosi di diabete gestazionale: esistono una serie di linee guida elaborate da vari gruppi di ricerca raggruppati in studi multicentrici o da associazioni internazionali di diabetologi riunitesi per discuterne. Per questo motivo potrebbe darsi che, a parità di valori, ad alcune donne venga diagnosticato diabete gestazionale e ad altre no.
Le principali associazioni di riferimento sono:
– Raccomandazioni dell’Organizzazione mondiale della sanità (World Health Organization, WHO) del 1999: test OGTT (test di tolleranza al carico orale di glucosio o “curva da carico”) con 75 g di glucosio misurando la glicemia a digiuno e dopo 2 ore con cut-off per la diagnosi pari o superiore a 140 mg/dl.
– Raccomandazioni del Gruppo di studio Indiano (Diabetes in Pregnancy Study Group of India, DIPSI): diagnosi di GDM posta a valori di glicemia superiori o uguali a 140 mg/dl dopo 2h dal test OGTT con 7 5g di glucosio.
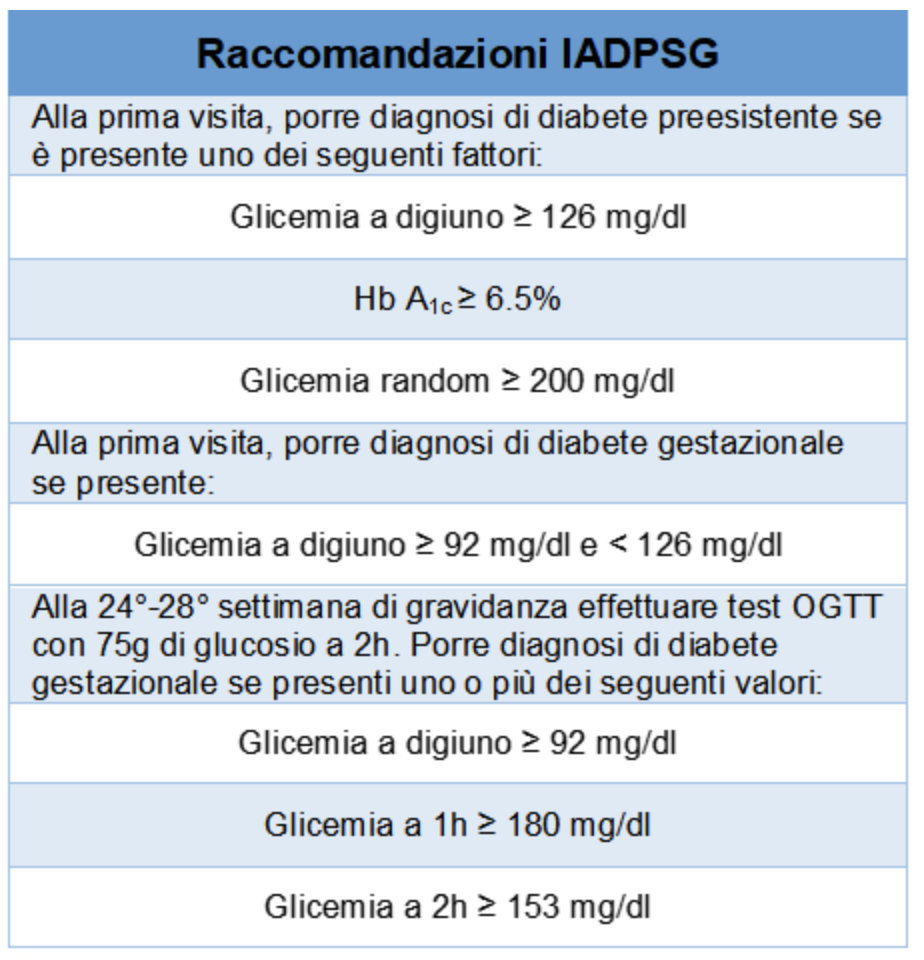
– Raccomandazioni del Gruppo di studio internazionale (International Association of Diabetes in Pregnancy Study Group, IADPSG) del 2008: basate sullo studio HAPO che ha analizzato 25.505 donne incinte con il test OGTT con 75 g di glucosio a 2h e ha messo in relazione i risultati con il successo della gravidanza, dimostrando una connessione tra i livelli di glicemia e gli eventi avversi prima durante e dopo il parto.
Di fatto queste raccomandazioni per la prima volta hanno correlato il diabete non diagnosticato prima e dopo la gravidanza come un concreto fattore di rischio per aborto.
– Linee guida IADPSG per la diagnosi del diabete gestazionale.
Interessante notare che, sebbene il diabete gestazionale sia spesso correlato a sovrappeso della donna, esso non è un criterio diagnostico: anche donne normopeso possono avere problemi di diabete in gravidanza,
Il trattamento del diabete gestazionelae
Il trattamento del diabete nel corso della gravidanza è essenzialmente basato su:
a) Un regime alimentare adeguato e bilanciato il cui obiettivo principale è quello di evitare picchi glicemici e consentire la fisiologica crescita del feto
b) Una regolare attività fisica che aiuti non solo a mantenere sotto controllo il peso ma anche per la sua azione positiva sul profilo endocrino e metabolico.
Alla paziente con diabete in gravidanza va quindi raccomandato un cambiamento dello stile di vita compatibile con il periodo gestazionale: è importante che si sensibilizzi la paziente a una dieta a basso carico glicemico, con pochissimi zuccheri e ricca di sostanze funzionali. Non si deve seguire dieta dimagrante!
È inoltre importante che la madre monitori regolarmente la glicemia a digiuno e dopo i pasti (automonitoraggio).
Solo in una piccola percentuale di casi (circa il 10%) è necessario far ricorso a una terapia farmacologica (insulina) per abbassare i livelli di glucosio post-prandiali, privilegiando in particolar modo gli analoghi rapidi dell’insulina che sembrano agire meglio (in maniera più veloce e lunga nel tempo) sul controllo della glicemia. Al contrario, si preferisce evitare la somministrazione di farmaci ipoglicemizzanti orali in quanto non sono ancora disponibili dati esaustivi riguardo i possibili effetti sul feto.
Microbiota e diabete
Nella maggior parte dei casi la dieta da sola è sufficiente a tenere sotto controllo i livelli di glicemia per questo essa rappresenta uno dei primi approcci di terapia per il GDM. La letteratura scientifica è ricca di dati che sottolineano il profondo legame tra la dieta e il microbiota intestinale e come esso a sua volta ne moduli il metabolismo e lo stato infiammatorio.
Per microbiota si intende l’insieme dei microrganismi che colonizzano il tratto intestinale umano e che in simbiosi con l’ospite (uomo) digeriscono gli alimenti producendo composti bioattivi che hanno effetto benefico sulla fisiologia dell’intero individuo e nel corso dell’intera esistenza. Non stupisce quindi che una composizione del microbiota alterata, condizione definita come disbiosi, sembri avere un ruolo chiave in molte malattie acute e croniche come quelle che interessano il metabolismo (diabete, obesità, insulino-resistenza).
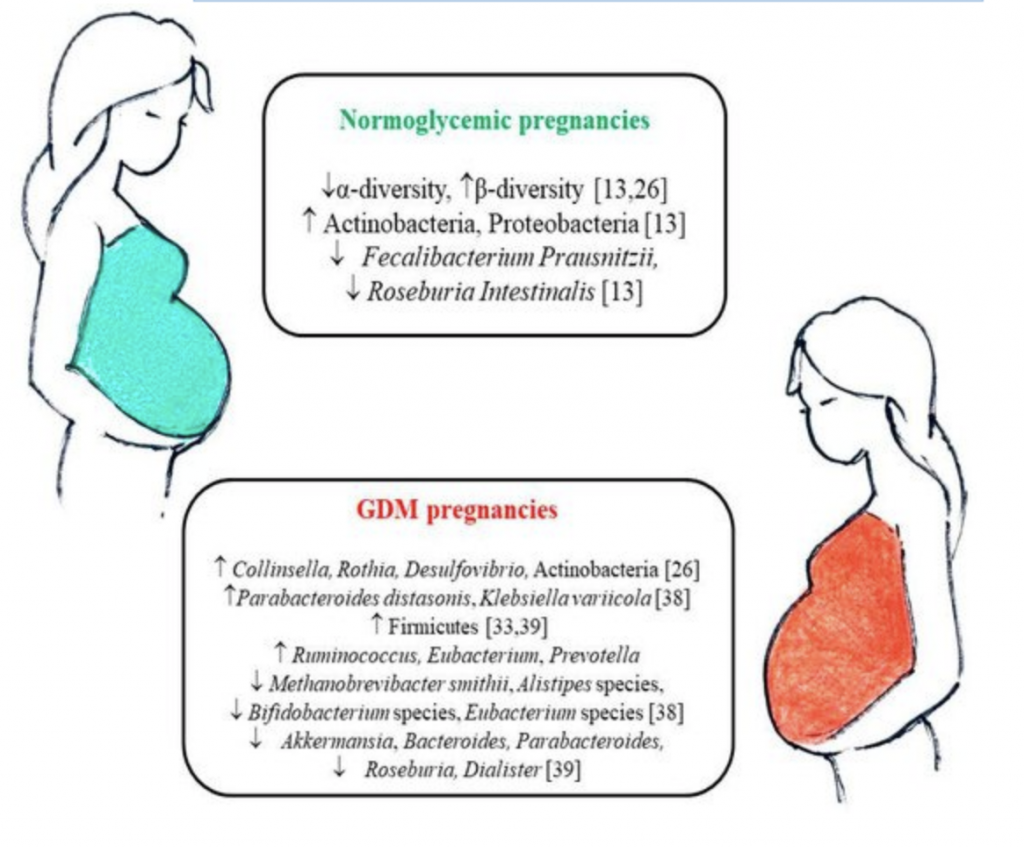
Microbiota in gravidanza: il maggior numero di cambiamenti si verifica nel primo trimestre con un aumento della varietà dei batteri (beta-diversità: misura del turnover delle specie inter-individuale) e una diminuzione della loro ricchezza (alfa-diversità: misura intra-individuale dell’abbondanza e numero delle specie presenti). I cambiamenti ormonali, immunologici e metabolici che avvengono nella madre sono atti a promuovere l’aumento di peso, l’aumento delle citochine proinfiammatorie circolanti e l’insulino resistenza che in particolare nell’ultimo trimestre ha lo scopo “fisiologico” di sostenere la crescita fetale e aumentare l’assorbimento dei nutrienti. Questi cambiamenti sono particolarmente accentuati nelle donne con GDM dove l’aumentato rilascio di insulina è la causa dell’intolleranza glucidica. Inoltre la popolazione microbica vede una prevalenza di specie come Roseburia e Akkermansia muciniphila che sono state associate anche al diabete mellito.
La domanda in questione è se il microbiota contribuisca o rappresenti la conseguenza dell’instaurarsi del GDM soprattutto alla luce di studi in cui a distanza di anni dal parto donne GDM positive e negative non mostrano alcuna differenza nella composizione del microbiota.
È invece accertato che il microbiota materno sia trasmesso alla prole e in particolare neonati di madri affette da diabete ricevono batteri specifici diversi da quelli di madri normoglicemiche per cui la modulazione del microbiota riveste una notevole importanza per la salute futura del nascituro.
La dieta materna come strategia di prevenzione
Storicamente il principale obiettivo della dieta per pazienti affette da GDM era la restrizione dei carboidrati con conseguente riduzione degli zuccheri in modo da limitare i livelli di glucosio post prandiale ed evitare l’esposizione del feto all’iperglicemia. Tuttavia, negli ultimi decenni sono apparsi alcuni dubbi riguardo questo tipo di restrizione e sulla sua modulazione in qualità piuttosto che in quantità. È emerso infatti che il principale impatto dei carboidrati nei soggetti diabetici è dovuto al loro carico glicemico e in seguito per la loro qualità, un fattore importante nell’influenzare la composizione del microbiota intestinale. In aggiunta, si è visto che una dieta povera di carboidrati ma ricca di grassi (come spesso accade in restrizione glucidica) è in grado di aumentare ulteriormente il numero di batteri pro-infiammatori (generi anaerobiche come Bacteroides) e favorire in questo modo l’insulino-resistenza. Al contrario, l’abbondanza di specie come i Bifidobacterium è associata a riduzione della glicemia e della colesterolemia.
Recenti studi hanno messo inoltre in evidenza il ruolo di un approccio personalizzato alla dieta delle pazienti GDM distinguendole in base al microbiota in due enterotipi principali:
– Bacteroides (tipo B) associati a diete povere di fibra e ricche di grassi
– Prevotella (tipo P), associati a una dieta basata su vegetali e ricca di carboidrati e fibra
È stato infatti visto come solo i soggetti del tipo P beneficiassero di una dieta ricca di fibre (beta glucani e arabinoxilani) al contrario del tipo B. Studi presenti in letteratura, hanno inoltre dimostrato una prevalenza del genere Prevotella nelle donne affette da GDM rispetto al resto della popolazione per cui indicazioni dietetiche specifiche dovrebbero suggerire il consumo di alimenti contenenti arabinoxilani e beta glucani tra i quali il frumento, l’orzo, la segale, l’avena, il sorgo, il mais, il miglio, lo psyllium e i semi di lino.
Uno studio pubblicato nel marzo 2019 ha cercato di evidenziare l’importanza della dieta sulla prevenzione del diabete gestazionale non solo per le donne a rischio ma anche per quelle che programmano una gravidanza e non considerate a rischio, in quanto esse rappresentano il 38% che poi lo manifestano.
In particolare è stato visto che donne con diagnosi successiva di diabete, avevano una dieta contraddistinta da alti livelli di acidi grassi saturi anche se il consumo di acidi grassi polinsaturi (PUFA) seppur noti per la loro azione protettiva nel diabete di tipo 2, non sembrano avere una relazione chiara con il diabete gestazionale. I ricercatori tuttavia, raccomandano come strategia di prevenzione una dieta caratterizzata da cereali, vegetali, frutta, pollame e pesce limitando il consumo di acidi grassi e zuccheri noti per la loro elevata carica glicemica, che abbassando la sensibilità dei tessuti all’azione dell’insulina ne riducono la fisiologica secrezione.
In accordo con un altro recentissimo studio, è stato visto come donne incinte con una dieta ricca di vegetali, frutta, frutta secca, olio extravergine di oliva, pesce, legumi e cereali mostrano una riduzione del rischio di sviluppare un diabete gestazionale o altre complicazioni legate alla gravidanza quali parto prematuro e/o cesareo, peso elevato del nascituro e preeclampsia. E non solo: la riduzione delle infezioni urinarie sembra essere direttamente associata al consumo di olio extravergine di oliva: l’idrossitirosolo in esso contenuto avrebbe un effetto benefico e anti-infiammatorio sul microbiota urinario.
Ad oggi, la nostra conoscenza del microbiota intestinale e della risposta alla dieta in gravidanza complicata dal diabete è decisamente limitata. Tuttavia, nel formulare lo schema nutrizionale ottimale per la paziente è importante tenere in considerazione i potenziali benefici della dieta sulla madre, sul feto e sul microbiota materno che, a sua volta, influenzerà il microbiota del nascituro.
Di fatto, si suggerisce alla paziente cui sia stata fatta diagnosi di diabete gestazionale di evitare il consumo di zuccheri e prodotti industriali in generale, privilegiando cereali integrali , ortaggi e frutta, grassi benefici da olio extravergine e frutta a guscio o semi oleosi. L’obiettivo è quello di normalizzare la glicemia, non di dimagrire, pertanto la dieta deve essere normocalorica e assecondare il periodo gestazionale.
In donne sovrappeso un simile approccio potrebbe rivelarsi vincente anche sul dimagrimento, al termine dell’allattamento.
Roberta Ranieri, PhD student Section of Hematology Department of Medicine University of Perugia